诊断:
1.结节性多动脉炎初发的临床表现各不相同,早期不易确诊。大多数患者有全身性表现如乏力、发热和体重下降等。如同时有皮肤损害,周围神经病以及肾脏病变等多系统受累则高度提示结节性多动脉炎的诊断。
风湿性多肌痛综合征或大关节受累的寡关节炎也可能是结节性多动脉炎早期的临床表现。提示结节性多动脉炎诊断的一些关键的临床表现为:
(1)全身性表现:发热,寒战,疲乏,体重下降,周身不适。
(2)关节痛或肌痛。
(3)多器官受累,包括。
①皮肤损害(紫癜,网状表斑,坏死性损伤,肢端坏死)。
②周围神经病变(多发性单神经炎)。
③尿沉渣异常,高血压。
虽然结节性多动脉炎的诊断主要根据临床表现,但活检和血管造影是确诊结节性多动脉炎的重要依据:①活检:如病理证实有中、小动脉的坏死性血管炎则提示本病的可能,但无特异性。活检的阳性率与取材部位有关。在有相应症状体征的器官和组织取材,阳性率相对较高。②血管造影:也无特异性,但可提示有无
系统性血管炎存在。
2.1990年美国风湿病协会提出了结节性多动脉炎的分类标准(表1)。1994年在美国Chapel Hill召开的国际血管炎会议又提出了结节性多动脉炎的定义标准,即:中、小动脉的坏死性炎症,无微动脉、毛细血管和小静脉受累,无肾小球肾炎。目前临床上主要参考这两个标准来诊断结节性多动脉炎。许多学者认为Chapel Hill会议制定的标准较狭窄,按这标准诊断,结节性多动脉炎的发病率非常低,因此它的临床实用性尚需进一步的研究。
3.1990年美国ACR关于PAN的分类(诊断)标准,符合下列标准中3条或3条以上者可确诊:
(1)体重下降≥4kg,除外节食或其他因素。
(2)网状青斑:四肢或躯干呈斑点及网状斑。
(3)睾丸疼痛或触痛:除外由于感染、外伤或其他原因所致。
(4)肌痛、无力或下肢触痛。弥漫肌痛(除外肩带肌和髋带肌)及肌无力或下肢肌触痛。
(5)单神经病或多神经病。
(6)舒张压≥12.0kPa(90mmHg)。
(7)肌酐、尿素氮升高:血肌酐≥132.7μmol/L(1.5mg/dl)或血尿素氮≥14.3mmol/L(40mg/dl)。
(8)乙型肝炎病毒:血清中检测到HBsAg或HbsAb。
(9)血管造影异常:包括内脏血管动脉瘤或阻塞,除外动脉硬化。
(10)中小动脉活检:病理示动脉壁内有粒细胞和(或)单核细胞浸润。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制
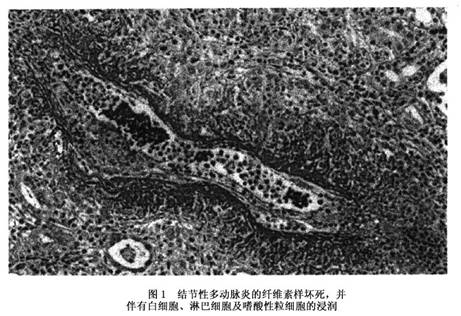
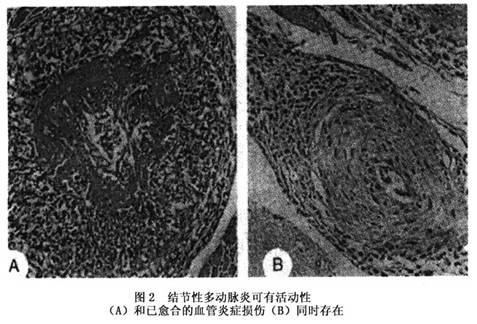


 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
.jpg)
 诊断
诊断
.jpg)
 鉴别诊断
鉴别诊断
.jpg)
 治疗
治疗
 预后
预后
.jpg)